GM AAV 패키징 서비스
- 효율적이고 생산적 / 비할 데 없는 품질과 생존력 / 다양한 AAV 벡터 등급 / 빠른 처리, 높은 순도, 향상된 활동성, 우수한 안전성
GVC AAV 생산 서비스
AAV는 유전자 치료 및 유전자 편집 작업에 안전하고 효율적인 바이러스 벡터로 알려져 있습니다. 바이러스 벡터는 in vivo 유전자 전달에 특히 적합합니다. AAV1.0, AAV2.0에서 AAV3.0까지 3세대 AAV의 개발과 함께, 다양한 조직 특이성을 가진 더 많은 인공 세로타입이 존재하여 원하는 장기를 특정 타겟팅할 수 있게 되었습니다.
GVC (GeneMedi Vector Core)는 연구부터 임상까지 다양한 AAV 벡터 등급을 보유하여, 과학적 및 임상 연구의 다양한 용도를 위한 다양한 수준의 AAV 벡터를 제공합니다. GVC AAV 벡터의 생산은 독자적인 최첨단 기술, 유연하고 원활한 생산 워크플로우 및 엄격한 품질 관리를 통해 효율적이고 생산적이며 높은 품질과 완전한 신뢰성을 갖추고 있습니다.
GeneMedi GVC는 귀하의 AAV 생산 및 AAV 프로세스 개발에 이상적인 파트너가 될 것입니다.
GVC 서비스의 AAV 종류
-
여러 세로타입: AAV1, 2, 3b, 4, 5, 6, 7, 8, 9, PHP.eB, PHP.B, PHP.S, rh10, DJ, DJ/8, AAV2.7m8, AAV2-retro, AAV8-1m/2m/3m, AAV2(Y444F), AAV2, AAV6.2FF, AAV-i.e, AAV-BR1, AAV-2i8, AAV-SIG, AAV-VEC, AAV-Myo, Anc80 등
-
싱글 스트랜드 AAV (ssAAV) 및 셀프 컴플리멘터리 AAV (scAAV)
-
프리메이드 AAV 입자 및 맞춤형 AAV 생산
GVC AAV 생산의 안정성
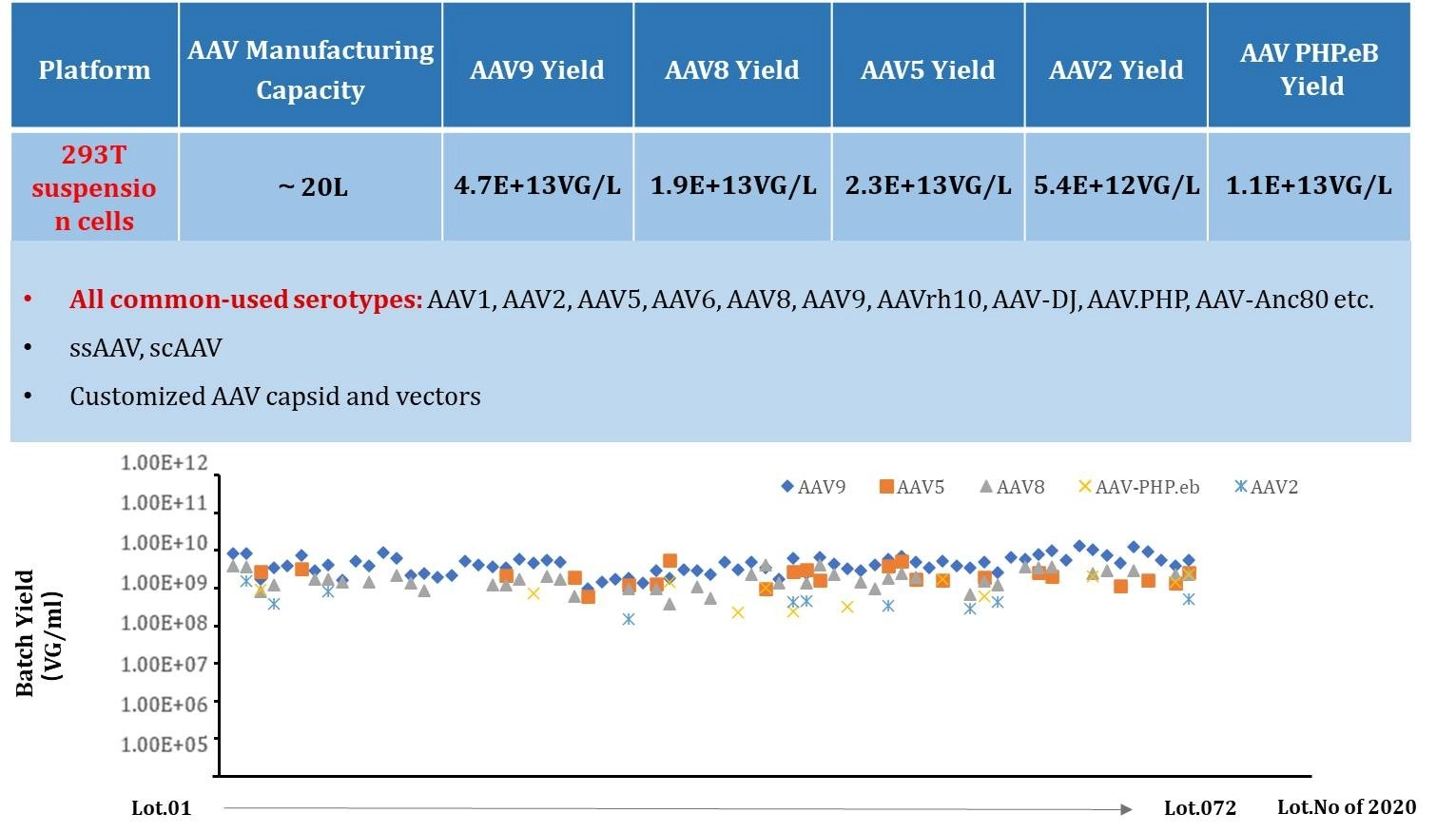
그림 1: 높은 수율의 일관된 AAV 생산 플랫폼
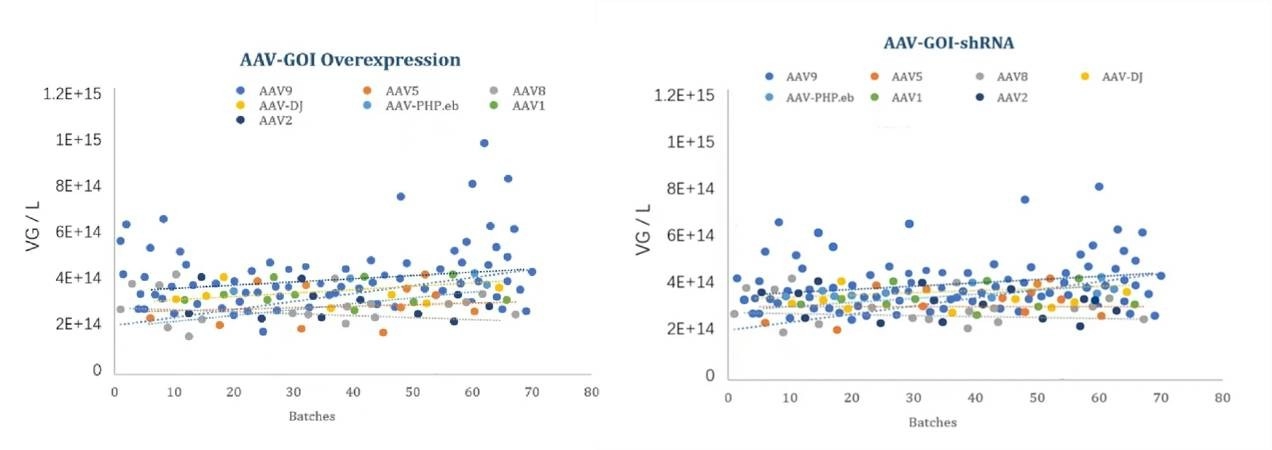
그림 2: 다양한 AAV 세로타입의 제조 배치 안정성
상류 공정 및 하류 공정
| 일시적 트리플 트랜스펙션 | 연구 등급-파일럿 | 연구 등급-표준 | GMP 유사 등급/GMP 등급 |
| 세포 유형 | 부착 | 부착 | 부유 |
| 세포 은행 | —— | —— | 추후 결정 |
| 무혈청 | N | N | Y |
| 플라스미드 은행 | N | N | Y |
| 정제 | 비정제 | CsCl 밀도 구배 | Clarification Tangential Flow Filtration Affinity chromatography Anion-Exchange (AEX) Chromatography |
| 규모 범위 | 1E+12 GC/~5E+13 GC | 5E+12 GC/~5E+14 GC | 추후 결정 |
분석 개발 및 품질 관리 (AD&QC)
- 일반 검사 (물리적 검사)
- 식별
- 내용 및 효능
- 순도
- 보안 검사
- 불순물
| QC 프로젝트 | 연구 등급-표준 | GMP 유사 등급/GMP 등급 | ||
| 방법 | 결과 | 방법 | 결과 | |
| 외관, 명확성 | 광검사 | 시각 검사 "입자가 없는 깨끗한 용액" |
외관, 명확성 | 시각 검사 "입자가 없는 깨끗한 용액" |
| 보이는 이물질 | —— | —— | 보이는 이물질 | 램프 검사 |
| 불용성 입자 | —— | —— | 불용성 입자 | 광 차단 방법 |
| pH 값 | —— | —— | pH 값 | pH 미터 제품 특정 |
| 삼투압 | —— | —— | 삼투압 | 냉동법 보조제 특정 |
| 적재량 | —— | —— | 적재량 | 체적법-USP/ChP 요구사항 준수 |
| QC 프로젝트 | 연구 등급-표준 | GMP 유사 등급/GMP 등급 | ||
| 방법 | 결과 | 방법 | 결과 | |
| AAV 유전체 서열 | —— | —— | 제한 효소 맵 분석 | 결과는 일치하지 않음 |
| —— | —— | 중합효소 연쇄 반응 (PCR) | ||
| —— | —— | 역전사 중합효소 연쇄 반응 (RT-PCR) | ||
| —— | —— | 핵산 서열 결정 | ||
| 캡시드 단백질 식별 | SDS-PAGE와 Western blot을 결합하여 캡시드 단백질 VP1/2/3을 식별 | VP1: VP2: VP3=1: 1: 10 | SDS-PAGE와 Western blot을 결합하여 캡시드 단백질 VP1/2/3을 식별 | VP1: VP2: VP3=1: 1: 10 |
| 완전한 바이러스 입자 식별 | —— | —— | 구조 분석, 입자 크기 분포, 전자 현미경 하에서의 굴절률 분석 | 응집체-TEM (음극 염색)≤10% |
| QC 프로젝트 | 연구 등급-표준 | GMP 유사 등급/GMP 등급 | ||
| 방법 | 결과 | 방법 | 결과 | |
| 바이러스 입자 역가 (V.P.) | —— | —— | ELISA | 결과 보고/~1E14 VP/ml |
| 유전체 역가 (V.G.) | QPCR | Q-PCR로 검출된 역가는 프로토콜 양 이상 | ddPCR | 보고된 결과/~1-5E13 VG/mL |
| 총 단백질 | —— | —— | BCA | 보고된 결과 |
| 단백질 발현 (세포) | —— | —— | ELISA/FIX | 추후 결정 |
| 감염 역가 (I.P.) | —— | —— | TCID50 | 결과 보고/1-5E11 TCID50/ml |
| 특정 활동 | —— | —— | 특정 활동 = 유전체 역가/감염 역가 | <100 |
| 효능 - 유전체 발현 | —— | —— | qPCR, ELISA, Western Blot에 기반한 세포의 in vitro mRNA 발현 또는 단백질 발현 검출 | 효능 내용 UV 0.8-1.2 mg/mL |
| 효능-활동 | —— | —— | 생체 기능 검사 | In Vitro Potency- (1-15 사이) vg/세포 |
| QC 프로젝트 | 연구 등급-표준 | GMP 유사 등급/GMP 등급 | ||
| 방법 | 결과 | 방법 | 결과 | |
| 캡시드 단백질 순도 검사 | SDS-PAGE 전기영동 및 은 염색 | SDS-PAGE ≥95%, VP1: VP2: VP3=1:1:10, 명확한 오염물질 발견되지 않음 | SDS-PAGE 전기영동 및 은 염색 | SDS-PAGE ≥95%, VP1: VP2: VP3=1:1:10, 명확한 오염물질 발견되지 않음 |
| 빈 쉘 비율 검출 | —— | —— | ddPCR/ ELISA | 결과 보고 |
| —— | —— | 투과 전자 현미경 (TEM) | 결과 보고 | |
| —— | —— | 분석용 초원심분리기 (AUC) | 결과 보고 | |
| 유전체 응집 검출 | —— | —— | 크기 배제 고성능 액체 크로마토그래피 (SEC-HPLC 방법) | 결과 보고 |
| QC 프로젝트 | 연구 등급-표준 | GMP 유사 등급/GMP 등급 | ||
| 방법 | 결과 | 방법 | 결과 | |
| 복제 가능한 아데노관련 바이러스(rcAAV)는 제품 안전성의 중요한 평가 지표입니다. | —— | —— | DNA 면역 블롯팅 (Southern blot) 및 qPCR | qPCR 음성 |
| 무균 검사 | 막 여과 | 성장 없음 | 막 여과 | 성장 없음 |
| 세균 내독소 검사 | 리물러스 시약 | 추후 결정 | 리물러스 시약 | LAL 시험<10 EU/ml |
| 마이코플라즈마 | 배양 방법 및 PCR 방법 | 추후 결정 | 배양 방법 및 PCR 방법 | 음성 |
| 외인성 인자 | —— | —— | 배양 | 음성 |
| 생물 부하 | —— | —— | 배양 | 결과 보고 |
| 비정상적 독성 검사 | —— | —— | 동물 실험 | ChP 요구사항 충족 |
| QC 프로젝트 | 연구 등급-표준 | GMP 유사 등급/GMP 등급 | ||
| 방법 | 결과 | 방법 | 결과 | |
| 도움이 되는 DNA 플라스미드 잔류물 | —— | —— | ddPCR/qPCR | ≤50ng/ml |
| 숙주 세포 DNA 잔류물 | —— | —— | ddPCR/qPCR | ≤50 ng/ml |
| 잔류 E1A/E1B DNA(복제/용량) | —— | —— | ddPCR/qPCR | ≤(5-10) x 10^4 복제/mL E1A; (5-10) x 10^4 복제/mL E1B |
| 숙주 세포 단백질 잔류물 | —— | —— | ELISA | ≤0.5ug/10E^12/ml |
| 우혈청 알부민 잔류물 | —— | —— | ELISA | ≤50ng/ml |
| 잔류 벤조네이스 | —— | —— | ELISA | ≤10 ng/ml |
| 특정 공정과 관련된 잔류물(예: 아이오딕산올, 트랜스펙션 시약, 친화 리간드, 트윈 20, 계면활성제 트리톤X100 등) | —— | —— | HPLC | 결과 보고 |
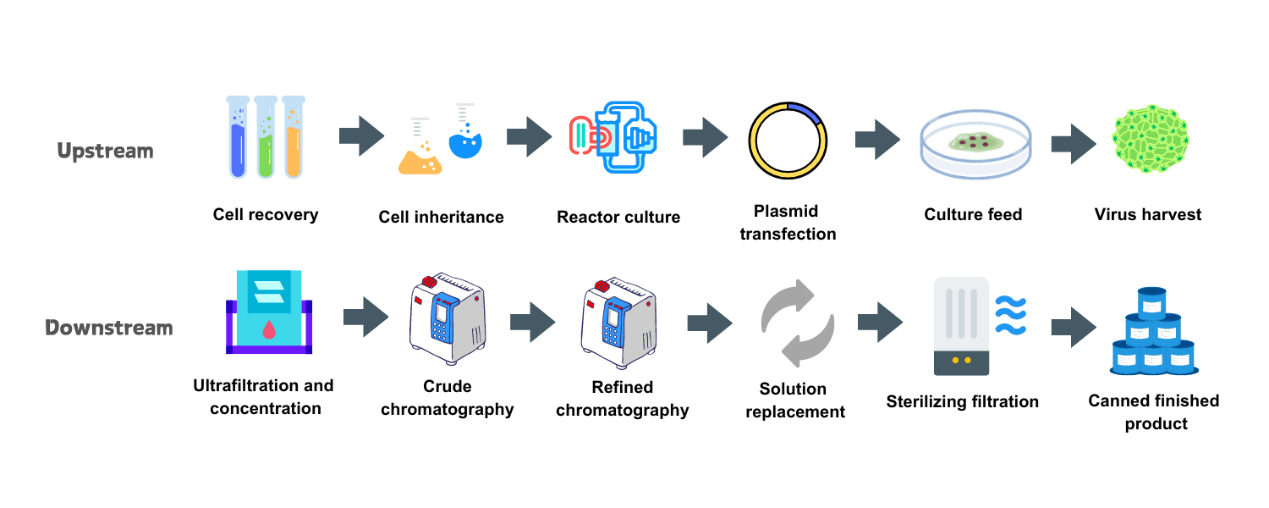
AAV 생산 워크플로우
GVC 소개
GVC (GM Vector Core)는 GeneMedi의 독자적인 QbD 바이러스 벡터 공정 개발 및 제조 플랫폼입니다. GVC에서 우리의 핵심 전문 지식은 아데노 관련 바이러스(AAV), 렌티바이러스, 아데노바이러스 및 VLP를 포함한 바이러스 벡터의 맞춤형 생산에 있습니다.
최첨단 시설은 확장 가능한 제조를 위해 설계되었으며, 연구 및 치료 요구를 충족시키는 고품질 바이러스 벡터 생산을 보장합니다. 우리의 전문 팀은 혁신적인 기술과 광범위한 산업 지식을 활용하여 고객에게 기대를 초과하는 맞춤형 솔루션을 제공합니다.
GVC는 신뢰할 수 있고 효율적인 바이러스 벡터 생산 서비스를 찾는 과학자와 의료 전문가에게 이상적인 파트너가 될 것입니다.
AAV 친화성 정제 효율성
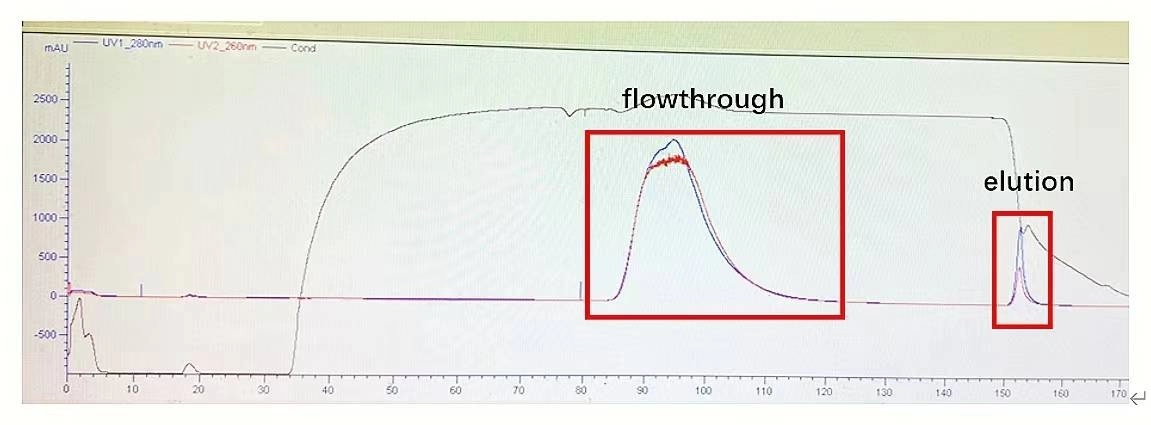
그림 3. AAV5 친화성 정제: AAV 친화성 크로마토그래피의 컬럼 효율성이 매우 좋습니다.
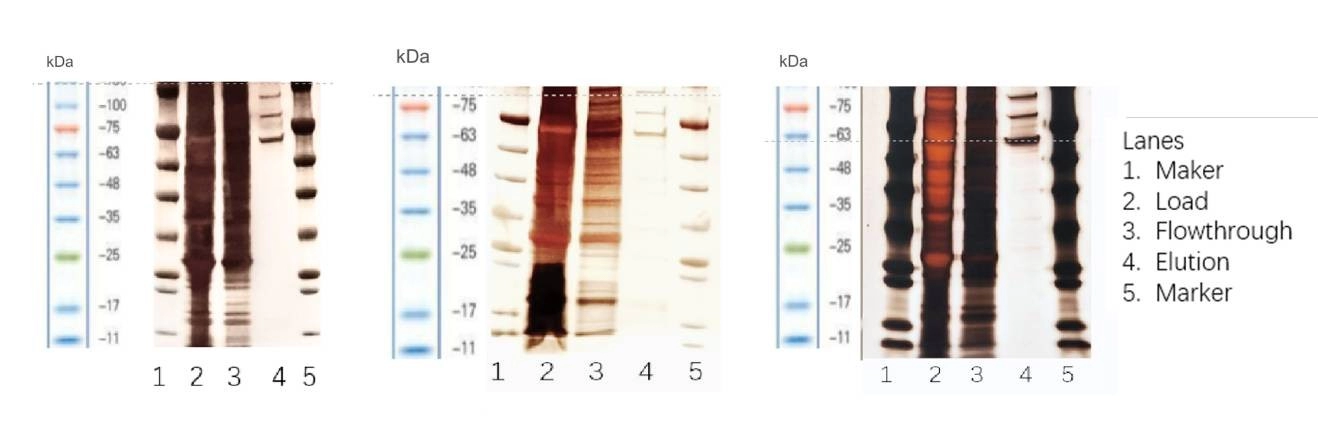
그림 4. 은 염색: AAV5/ AAV8/ AAV2 친화성 크로마토그래피 후 순도가 높습니다.
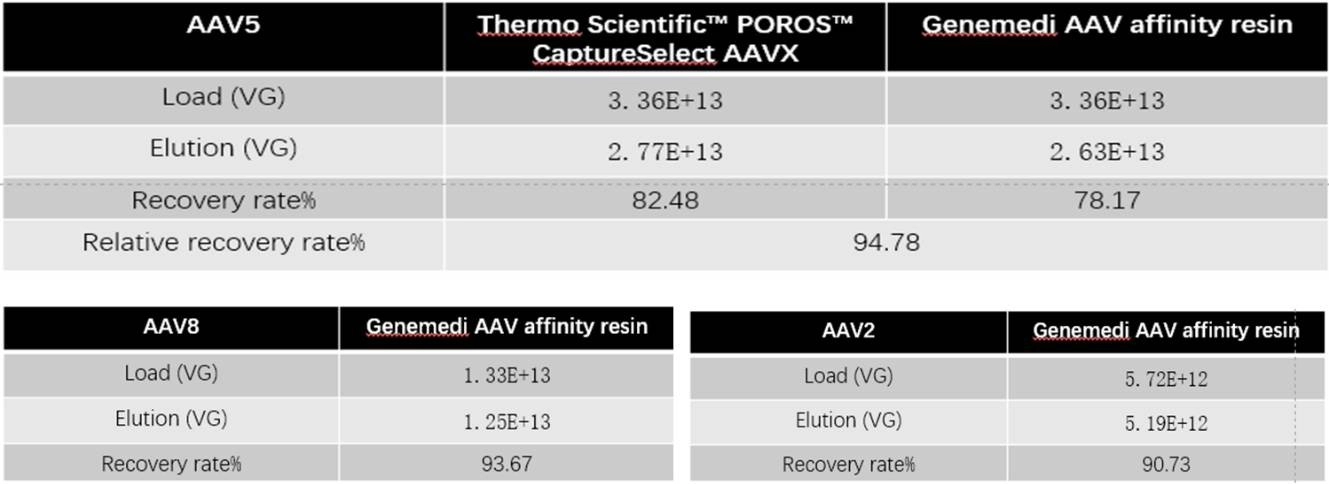
표 1: ddPCR은 Thermo Scientific™ POROS™ CaptureSelect AAVX와 역가 비교: AAV 친화성 크로마토그래피의 회수율이 유사합니다.
AAV 효능 증대
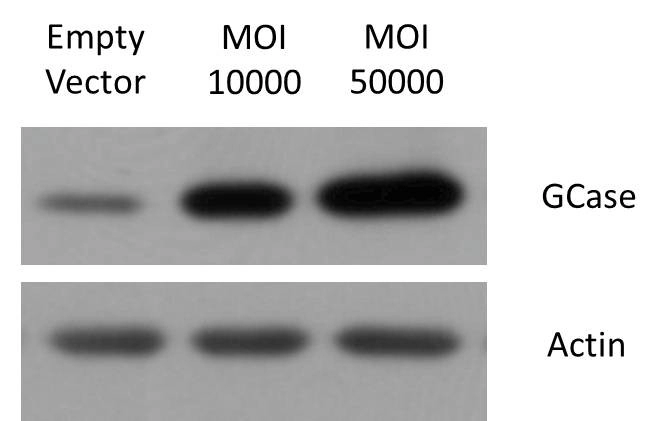
그림 5. AAV 효능. WB 결과는 과발현된 바이러스가 단백질 함량을 크게 증가시킬 수 있음을 보여줍니다.
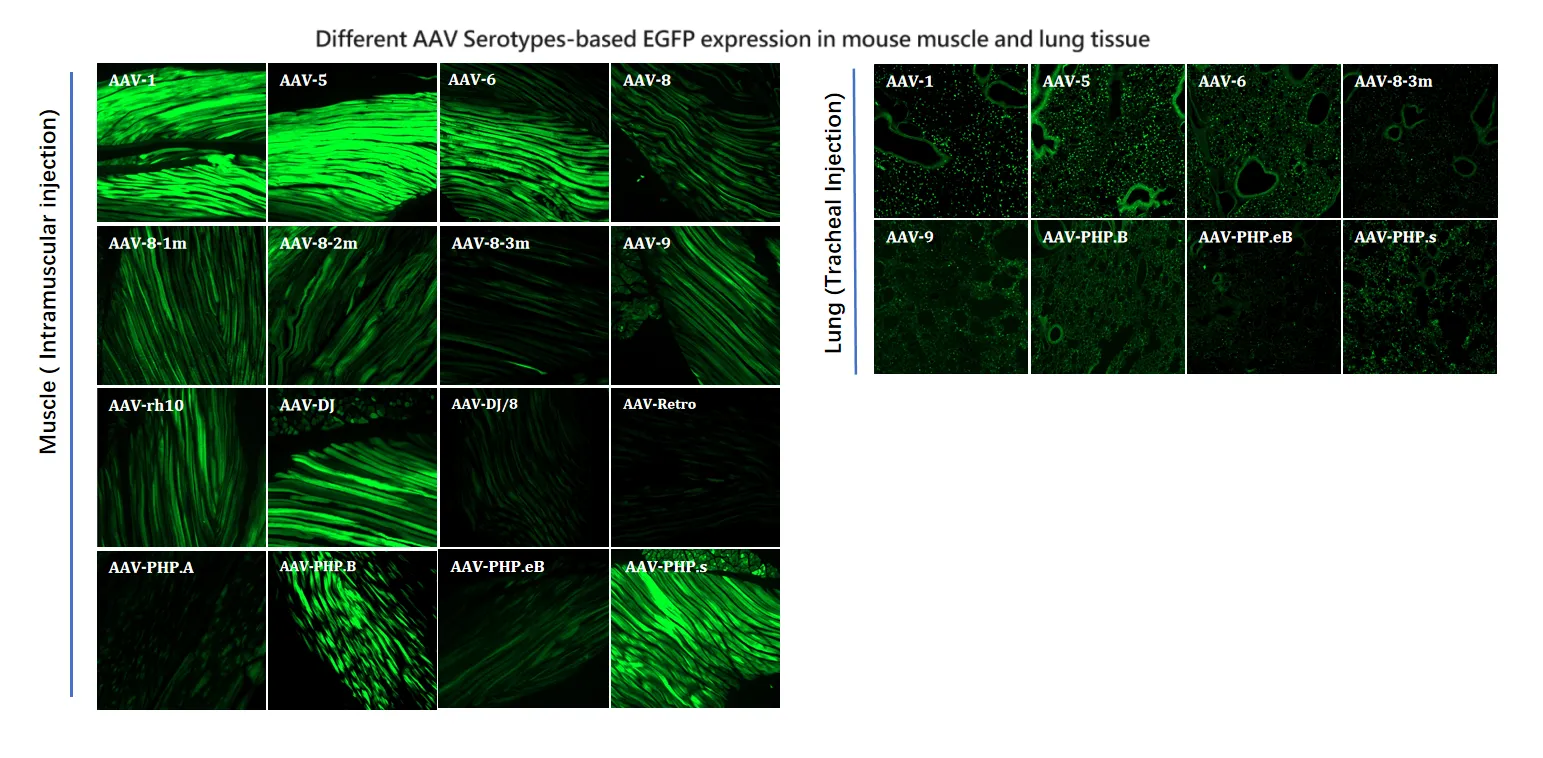
그림 6. 다양한 AAV 세로타입 기반의 EGFP 발현이 마우스 근육 및 폐 조직에서 나타납니다.
사례 연구 1: 마우스 해마에서 AAV 매개 UROC1-RNAi
혁신적인 연구에서 GeneMedi의 AAV 벡터는 마우스 해마에 UROC1-RNAi를 전달하는 데 사용되었으며, 이는 신경과학 연구의 진보에 있어 우리 제품의 중요한 역할을 입증합니다. 이 응용은 특정 뇌 영역을 타겟팅하는 AAV 벡터의 정밀성과 효율성을 강조하여 신경학적 상태를 연구하고 치료하는 새로운 길을 열어줍니다.
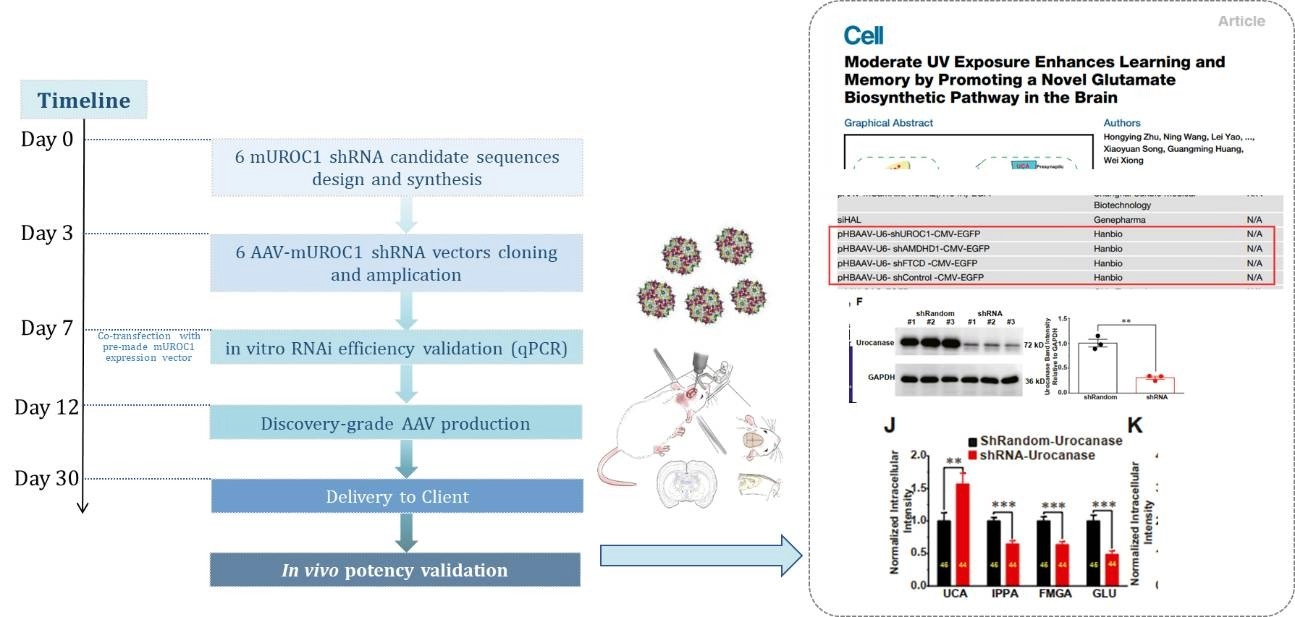
그림 6. AAV 세로타입의 근육 내 주사 후 형광 수준(4주). RC1, RC5, RC6, 및 PHP. s 감염이 가장 좋으며, 조직에서 형광이 가시적입니다; DJ, PHP 형광 현미경 B에서 더 밝습니다; 나머지 세로타입들은 다양한 정도의 감염 효과를 보이지만, 앞서 언급한 6개보다는 훨씬 약합니다.
사례 연구 2: 심장 특이적 AAV 발현 벡터 개발
우리는 AAV 카세트 최적화에서의 역량을 통해 심장 특이적 발현 벡터를 개발하며, 유전자 치료에 대한 맞춤형 접근 방식을 강조합니다. 이 성과는 목표 조직에서의 유전자 발현을 정밀하게 제어할 수 있는 프로모터 최적화에 대한 우리의 전문성을 입증하며, 이는 치료 성공과 특이성에 중요합니다.
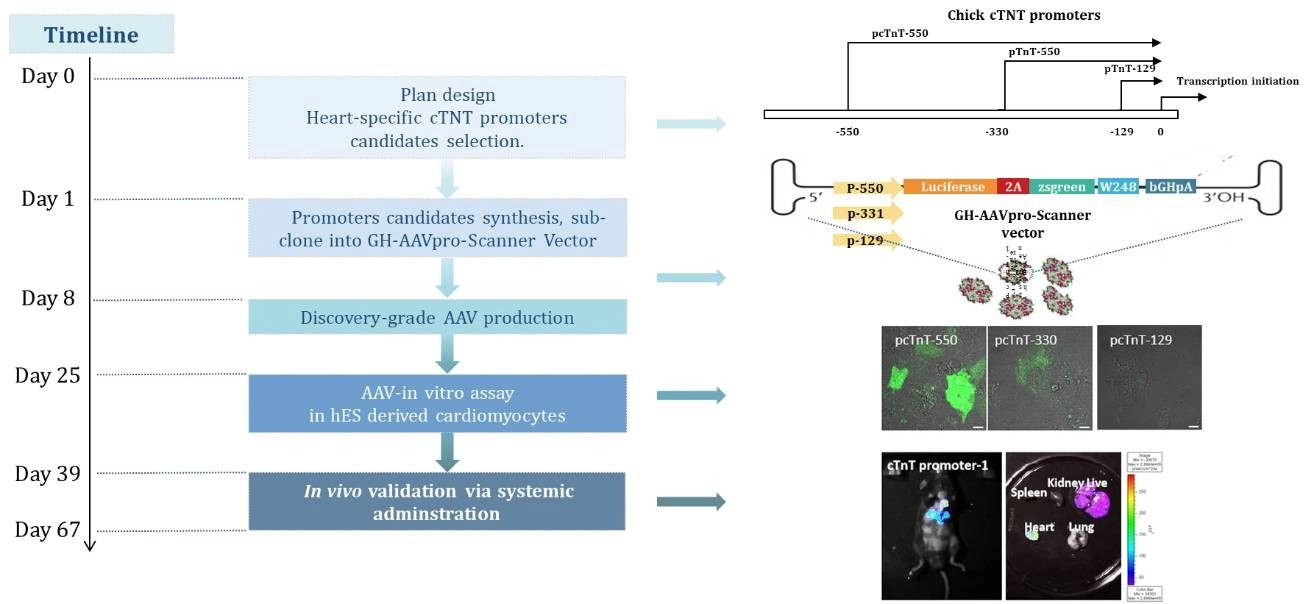
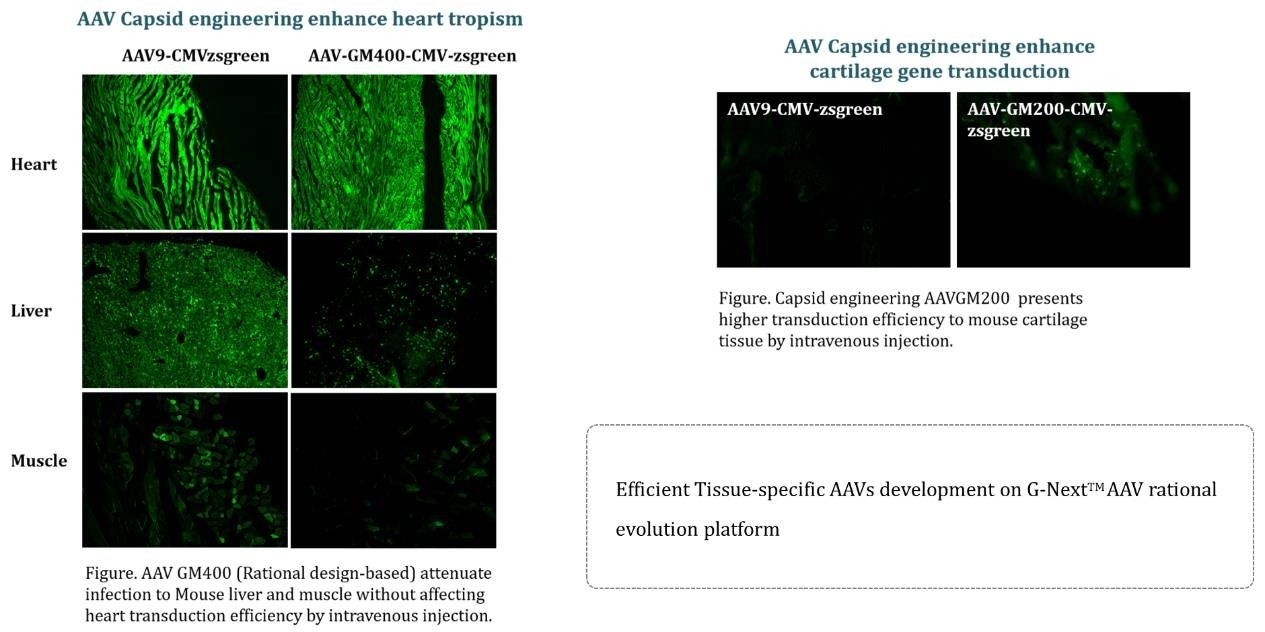
사례 연구 3: G-Next™에서 개발한 엔지니어링된 AAV 벡터의 우수한 조직 특이성
GeneMedi의 G-Next™ 플랫폼에서 개발된 엔지니어링된 AAV 벡터는 우수한 조직 특이성을 보여주며, 벡터 설계에서 우리의 혁신적 우위를 입증합니다. 이 진보는 특정 조직으로의 유전자 전달의 정밀성을 향상시키고 비표적 효과를 줄여 유전자 치료의 치료 잠재력을 높입니다. 혁신과 품질에 대한 우리의 헌신은 GeneMedi를 유전자 치료 분야의 선두주자로 만들며, 개인 맞춤형 의학의 가능성을 추진합니다.
인용 및 출판물
| 인용 및 출판물 |




 Facebook
Facebook LinkedIn
LinkedIn Twitter
Twitter
