ADC 약물 개발에서 PK 연구의 항 페이로드 항체
ADC(항체-약물 결합체)에 대한 항 페이로드 항체는 유리된 세포 독성 약물을 중화하고, 비표적 효과를 줄임으로써 안전성과 유효성을 향상시키는 것을 목표로 합니다. 이러한 항체는 정밀한 약물 전달을 촉진하고, 치료 프로파일을 개선하며, 약물 모니터링을 가능하게 합니다. 이는 맞춤형 치료 전략의 잠재력을 지닌 표적 암 치료의 중요한 발전을 의미합니다.
ADC(항체-약물 결합체)에 대한 항 페이로드 항체는 유리된 세포 독성 약물을 중화하고, 비표적 효과를 줄임으로써 안전성과 유효성을 향상시키는 것을 목표로 합니다. 이러한 항체는 정밀한 약물 전달을 촉진하고, 치료 프로파일을 개선하며, 약물 모니터링을 가능하게 합니다. 이는 맞춤형 치료 전략의 잠재력을 지닌 표적 암 치료의 중요한 발전을 의미합니다.
| Cat No. | Payload | Product Name | Fc | Technical Information | Products Information |
| GTU-Bios-Maytansinoids-Ab | DM1/DM4 | Anti-DM1/DM4 monoclonal antibody(mAb) | hFc/mFc | More | Details |
| GTU-Bios-Auristatin-Ab-01 | MMAE/MMAF | Anti-MMAE/MMAF monoclonal antibody(mAb) | hFc/mFc | More | Details |
| GTU-Bios-Auristatin-Ab-02 | MMAE (Specific) | Anti-MMAE (Specific) monoclonal antibody(mAb) | hFc/mFc | More | Details |
| GTU-Bios-DXd-Ab | DXd/Exatecan | Anti-DXd&Exatecan monoclonal antibody(mAb) | hFc/mFc | More | Details |
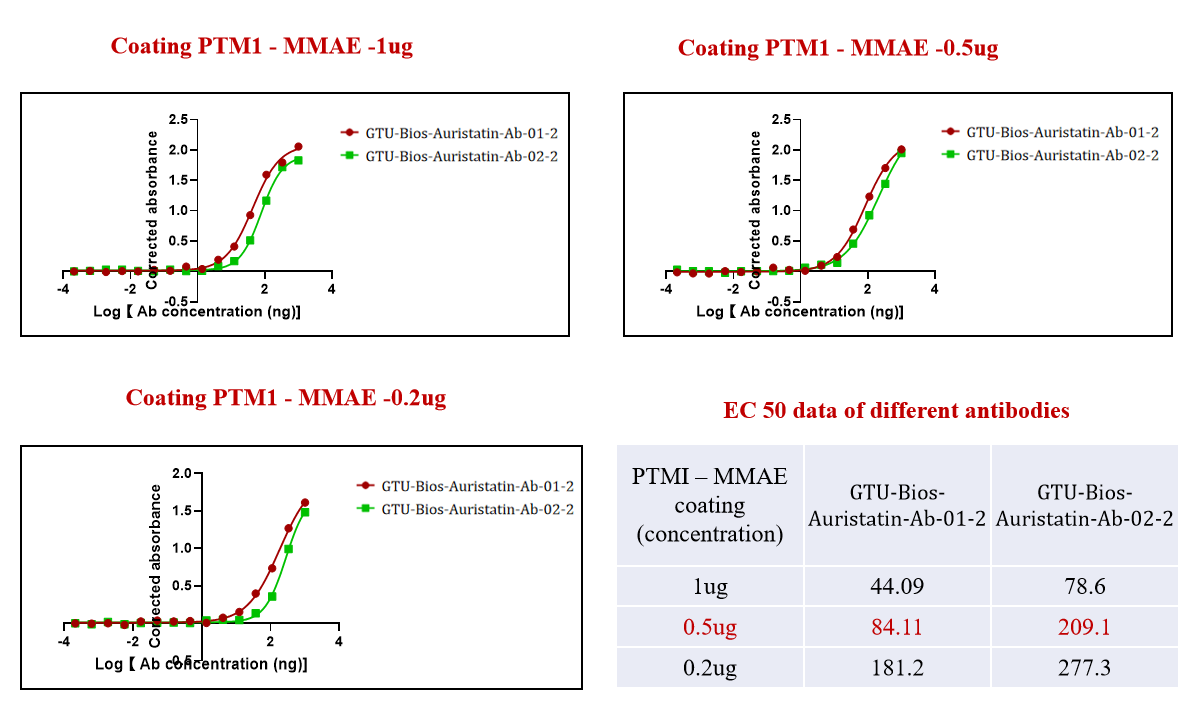
그림 1. GMP-Bios-MMAE-Ab-2 및 GMP-Bios-MMAE-Ab-3은 ADC(PTM-1 MMAE)와 적극적으로 결합했습니다.
그림 1은 GeneMedi의 GMP-Bios-MMAE-Ab-2 및 GMP-Bios-MMAE-Ab-3이 ADC(PTM-1 MMAE)와 적극적으로 결합하는 효능을 보여줍니다. 이는 MMAE 기반 ADC와 효과적으로 결합하기 위해 맞춤 제작된 고품질 항체를 생산하는 GeneMedi의 헌신을 강조합니다.
그림에서 보여주는 강력한 결합은, 항체-약물 결합체 (ADC)의 개발에서 GeneMedi의 전문 지식을 강조합니다. 이는 표적 약물 전달의 중요한 요소입니다.
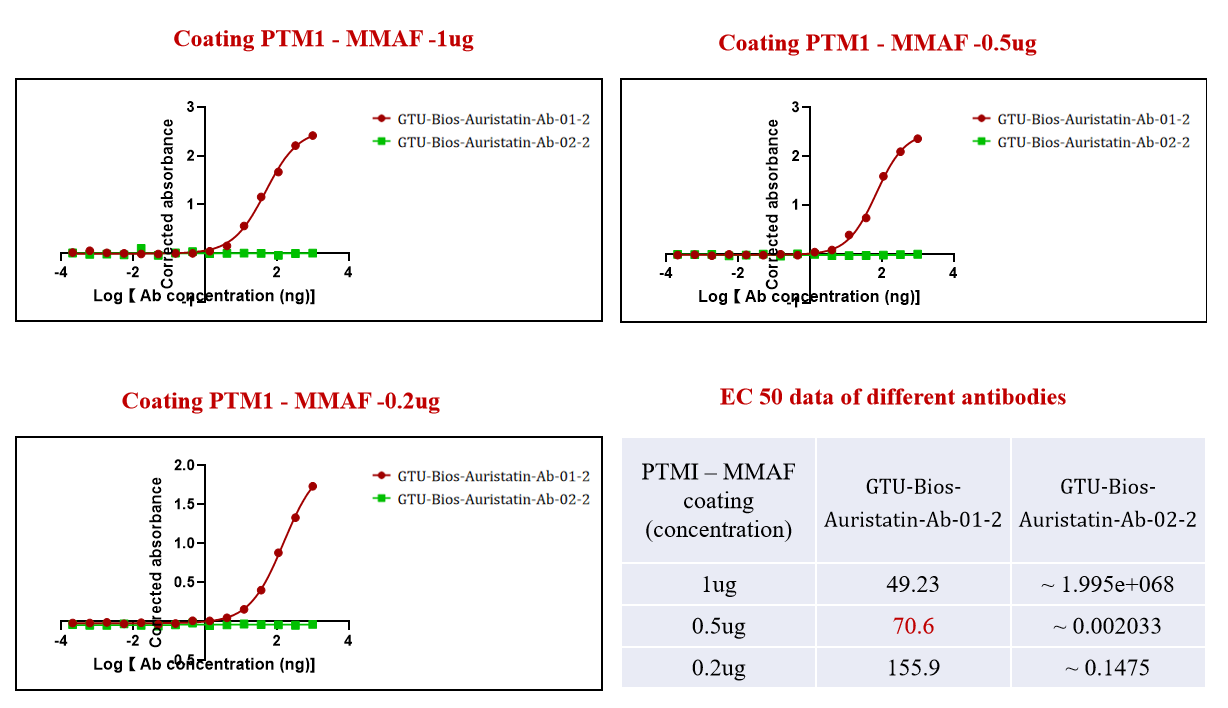
그림 2. GMP-Bios-MMAE-Ab-2은 ADC(PTM-1 MMAF)와 적극적으로 결합했습니다. 반면 GMP-Bios-MMAE-Ab-3는 MMAF와 결합하지 않았습니다.
그림 2에서는, GMP-Bios-MMAE-Ab-2이 ADC(PTM-1 MMAF)와 성공적으로 결합한 반면, GMP-Bios-MMAE-Ab-3는 결합하지 않는 특이성을 보여줍니다. 이러한 특이성은 MMAE를 포함하는 ADC의 정확한 표적화를 보장하고, 부작용을 최소화하는 데 중요합니다.
GeneMedi가 특정 약물 페이로드에 선택적으로 결합하도록 항체를 맞춤 제작하는 능력은, 연구자들에게 정밀 의학 응용 프로그램을 위한 신뢰할 수 있는 도구를 제공하는 항체 공학의 숙련도를 보여줍니다.
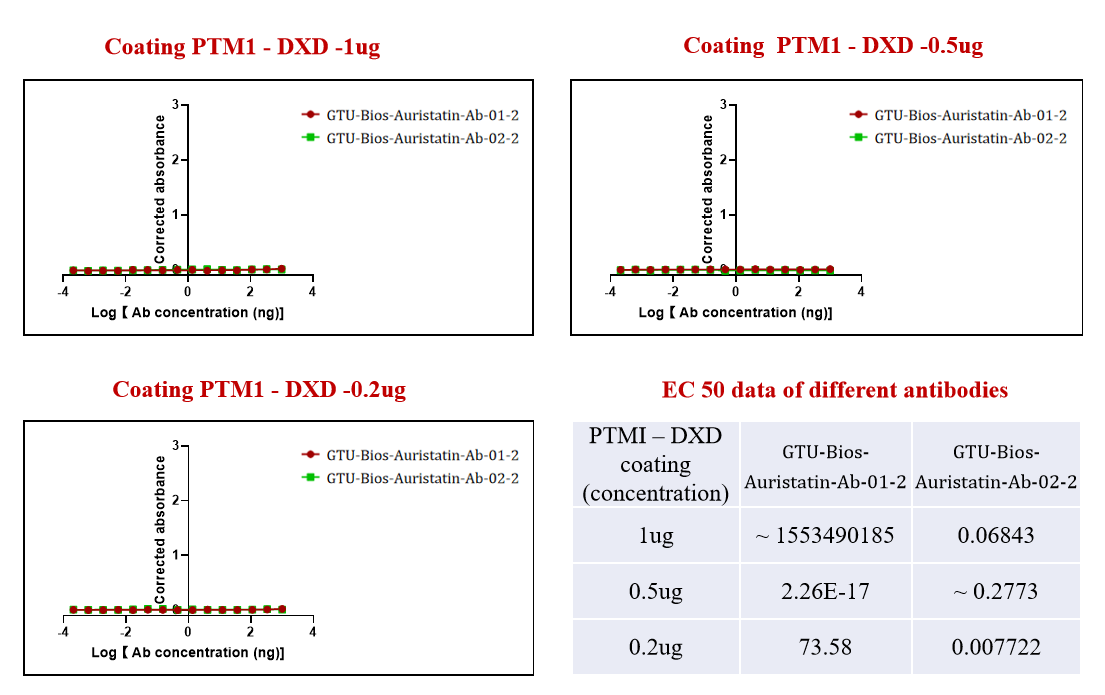
그림 3. GMP-Bios-MMAE-Ab-2 및 GMP-Bios-MMAE-Ab-3는 DXD로 결합된 ADC와 결합하지 않았습니다.
그림 3은 GeneMedi의 항체 특이성의 또 다른 측면을 보여주며, GMP-Bios-MMAE-Ab-2 및 GMP-Bios-MMAE-Ab-3 중 어떤 것도 DXD로 결합된 ADC와 결합하지 않는 것을 보여줍니다. 이 데이터는 불필요한 페이로드와의 간섭을 최소화하기 위해 높은 선택성을 갖춘 항체를 생산하는 GeneMedi의 헌신을 강조합니다.
교차 반응성이 최소인 항체를 제공함으로써, GeneMedi는 연구자들에게 타겟 암 치료를 위한 ADC 설계와 최적화를 위한 정확한 도구를 제공하여, 생의학 연구와 임상 응용의 최전선을 발전시킵니다.
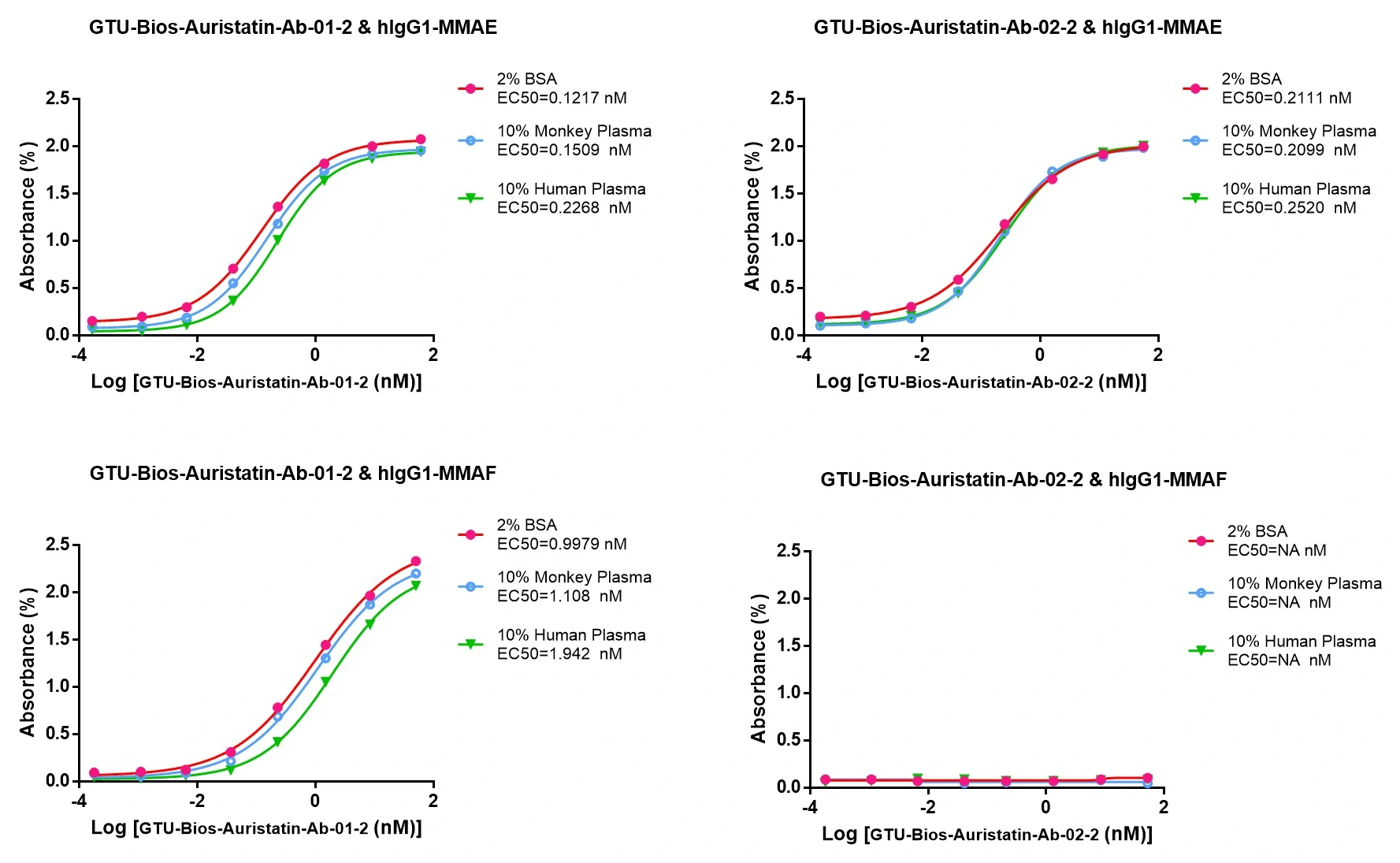
GTU-Bios-Auristatin-Ab-01-2 및 GTU-Bios-Auristatin-Ab-02-2는 인간과 원숭이를 포함한 약물동태(PK) 연구에 사용될 수 있습니다.
GTU-Bios-Auristatin-Ab-01-2는 인간과 원숭이 PK 연구에서 최소한의 영향을 미치며 무시할 수 있는 수준으로 간주될 수 있습니다. GTU-Bios-Auristatin-Ab-02-2는 이 PK 연구에서 GTU-Bios-Auristatin-Ab-01-2보다 더 적은 영향을 미칩니다. GTU-Bios-Auristatin-Ab-01-2와 GTU-Bios-Auristatin-Ab-02-2는 모두 인간과 원숭이 PK 실험에 적합합니다.
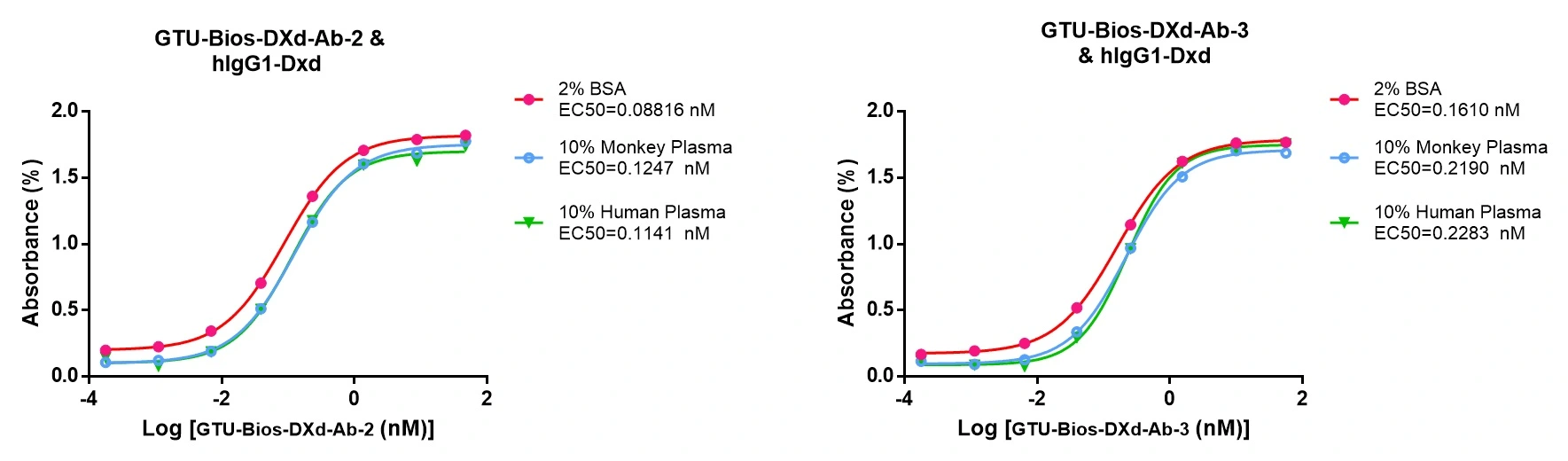
그림 2. GTU-Bios-DXd-Ab는 인간과 원숭이를 포함한 약물동태(PK) 연구에 최소한의 영향을 미칩니다.
GTU-Bios-DXd-Ab는 인간과 원숭이를 포함한 PK 연구에서 최소한의 영향을 보여, 이러한 실험에서 적절하게 사용할 수 있습니다.
항체-약물 결합체(ADC, Antibody-Drug Conjugates)의 "항 페이로드 항체" 개념은 ADC 치료의 개발 및 최적화에 있어서 독특한 전략을 포함합니다. 일반적으로, ADC는 화학적 링커를 통해 항체에 결합된 세포독성 약물(페이로드)로 구성됩니다. ADC의 항체 부분은 암세포의 특정 항원을 표적으로 하여, 이러한 세포에 세포독성 페이로드를 직접 전달하여 정상 세포를 보호하면서 이를 파괴합니다.
반면, "항 페이로드 항체"는 페이로드 분자를 인식하고 결합하도록 설계되었습니다. 이것은 여러 목적을 가질 수 있습니다:
안전성 및 독성 관리: 체내에서 비특이적으로 방출될 수 있는 자유 페이로드 분자에 결합함으로써, 이러한 항체는 오프 타겟 독성을 줄여 ADC 치료의 안전성 프로파일을 향상시킬 수 있습니다.
정밀도 향상: 연구에서 페이로드의 생체 내 분포와 제거를 더 잘 이해하기 위해 사용될 수 있으며, 보다 효율적이고 표적화된 ADC 설계로 이어질 수 있습니다.
약물 모니터링: 항 페이로드 항체는 환자의 시스템 내에서 약물 수준을 모니터링하는 분석을 개발하는 데 중요할 수 있으며, 맞춤형 투여량 조정을 가능하게 합니다.
이 아이디어는 아직 이 분야에서는 새롭지만, 항 페이로드 항체의 개발은 암 치료에서 부작용을 최소화하면서 치료 효과를 극대화하는 것을 목표로 하는 ADC 기술을 더욱 정교화하는 혁신적인 접근 방식을 나타냅니다.

