ADC 약물 개발에서 PK 연구에서 Anti-MMAE/MMAF 페이로드 항체의 사용
ADC(항체-약물 접합체) 약물 개발에서 약물 동태학(PK) 연구는 항체, 링커 및 세포 독성 약물을 포함한 ADC 및 그 구성 요소의 체내 행동을 이해하는 데 매우 중요합니다. 세포 독성 페이로드로 모노메틸 오리스타틴 E(MMAE) 또는 모노메틸 오리스타틴 F(MMAF)를 사용하는 ADC에 중점을 둘 때, anti-MMAE/MMAF 항체가 중요한 역할을 할 수 있습니다.
| Cat No. | Product Description | Fc | Products Information |
| GTU-Bios-Auristatin-Ab-01 | Anti-MMAE/MMAF monoclonal antibody | hFc/mFc | Details |
| GTU-Bios-Auristatin-Ab-02 | Anti-MMAE monoclonal antibody | hFc/mFc | Details |
응용
경쟁적 면역측정법(Competitive ELISA) 및 기타 면역측정법,
항체-약물 접합체(ADC)의 MMAE 페이로드에 대한 PK & PD 분석
특징
순도: ≥95% (SDS-PAGE)
높은 친화도와 특이성 검증
ADC 결합 분석을 통해 높은 민감도 확인
GeneMedi의 GMP-Bios-Auristatin-Ab: MMAE 및 MMAF 기반 ADC와의 정밀 결합
GeneMedi의 GTU-Bios-Auristatin-Ab-01-2는 MMAE 또는 MMAF 페이로드를 포함하는 ADC와의 강력한 결합 친화성을 보여주며, 표적 약물 전달에서의 다재다능함을 강조합니다. 반면, GTU-Bios-Auristatin-Ab-02-2는 MMAE 기반 ADC에 대한 독점적인 특이성을 보여주며, 최소한의 오프 타겟 효과로 정밀한 타겟팅을 보장합니다. 또한, 두 항체 모두 DXD와 결합된 ADC와는 결합하지 않아 GeneMedi의 최적화된 치료 결과를 위해 특수 설계된 고선택성 항체의 제조에 대한 헌신을 강조합니다.
- 그림 1: 코팅 PTM-1 MMAE
- 그림 2: 코팅 PTM-1 MMAF
- 그림 3: 코팅 PTM-1 DXD
- 그림 4: 약물 동태 (PK) 연구
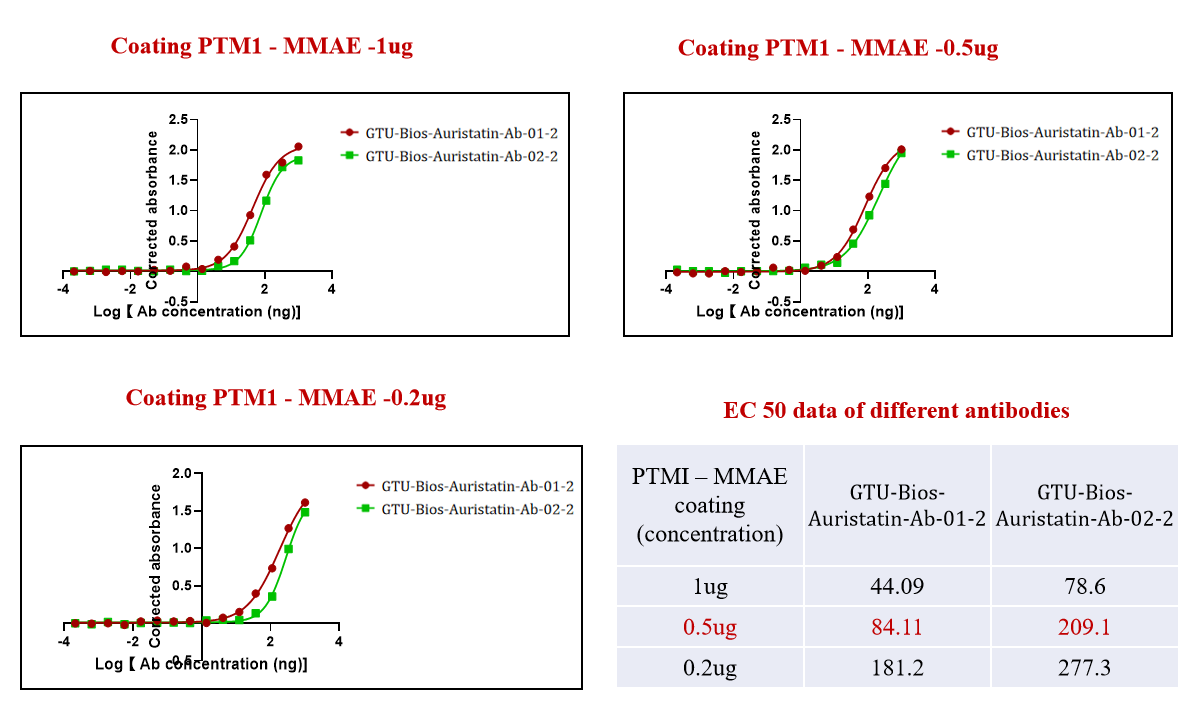
그림 1. GTU-Bios-Auristatin-Ab-01-2와 GTU-Bios-Auristatin-Ab-02-2가 ADC (PTM-1 MMAE)와 적극적으로 결합했습니다.
그림 1은 GeneMedi의 GTU-Bios-Auristatin-Ab-01-2와 GTU-Bios-Auristatin-Ab-02-2가 ADC (PTM-1 MMAE)와 적극적으로 결합하는 효능을 보여줍니다. 이는 MMAE 기반 ADC와의 효과적인 접합을 위해 맞춤 제작된 고품질 항체를 생산하는 GeneMedi의 헌신을 강조합니다.
그림에 나타난 강력한 결합은 항체-약물 접합체(ADC) 분야에서 GeneMedi의 전문성을 입증하며, 이는 표적 약물 전달에 최적화된 항체 개발의 중요한 측면입니다.
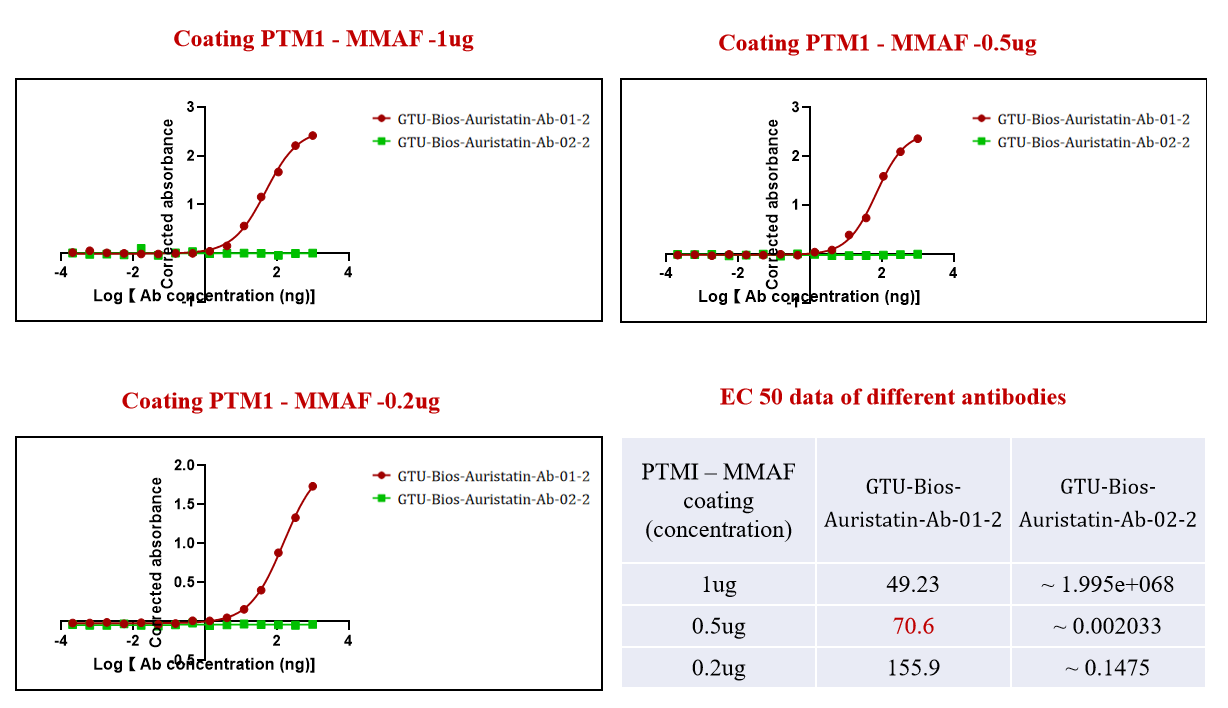
그림 2. GTU-Bios-Auristatin-Ab-01-2는 ADC (PTM-1 MMAF)와 적극적으로 결합했지만, GTU-Bios-Auristatin-Ab-02-2는 MMAF와 결합하지 않았습니다.
그림 2는 GTU-Bios-Auristatin-Ab-01-2가 ADC (PTM-1 MMAF)와 성공적으로 결합하는 동안 GTU-Bios-Auristatin-Ab-02-2는 결합하지 않는다는 점에서 GeneMedi의 항체 특이성을 보여줍니다. 이러한 특이성은 MMAE를 포함한 ADC의 표적 정확성을 보장하여 치료 효능을 높이고 비표적 효과를 최소화하는 데 중요합니다.
GeneMedi가 각기 다른 약물 페이로드와 선택적으로 결합하는 항체를 맞춤 제작할 수 있는 능력은 항체 엔지니어링에 있어 그들의 숙련도를 나타내며, 연구자들에게 정밀 의학 응용에 신뢰할 수 있는 도구를 제공합니다.
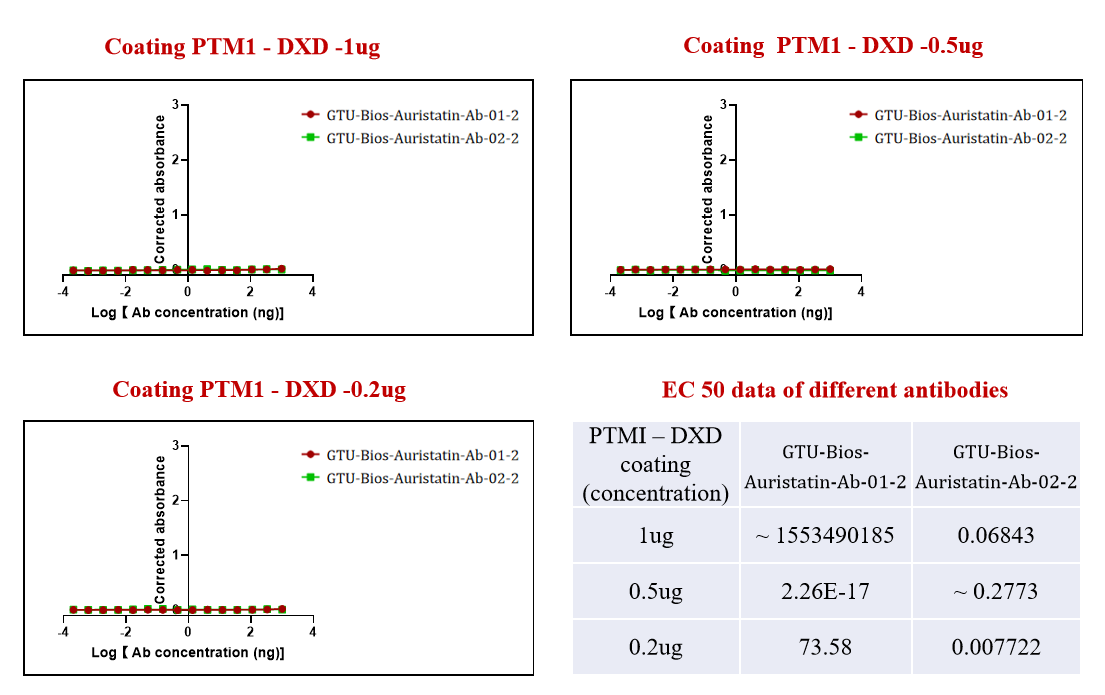
그림 3. GTU-Bios-Auristatin-Ab-01-2와 GTU-Bios-Auristatin-Ab-02-2가 DXD로 접합된 ADC와 결합하지 않았습니다.
그림 3은 GeneMedi의 항체 특이성의 또 다른 측면을 보여주며, GTU-Bios-Auristatin-Ab-01-2와 GTU-Bios-Auristatin-Ab-02-2가 DXD로 접합된 ADC와 결합하지 않는다는 것을 나타냅니다. 이 데이터는 바람직하지 않은 페이로드와의 간섭을 최소화하는 고선택성 항체를 생산하기 위한 GeneMedi의 헌신을 강조합니다.
교차 반응이 거의 없는 항체를 제공함으로써, GeneMedi는 연구자들에게 암 치료를 위한 ADC 설계 및 최적화에 있어 정밀한 도구를 제공하며, 궁극적으로 생의학 연구 및 임상 응용의 최전선으로 나아가고 있습니다.
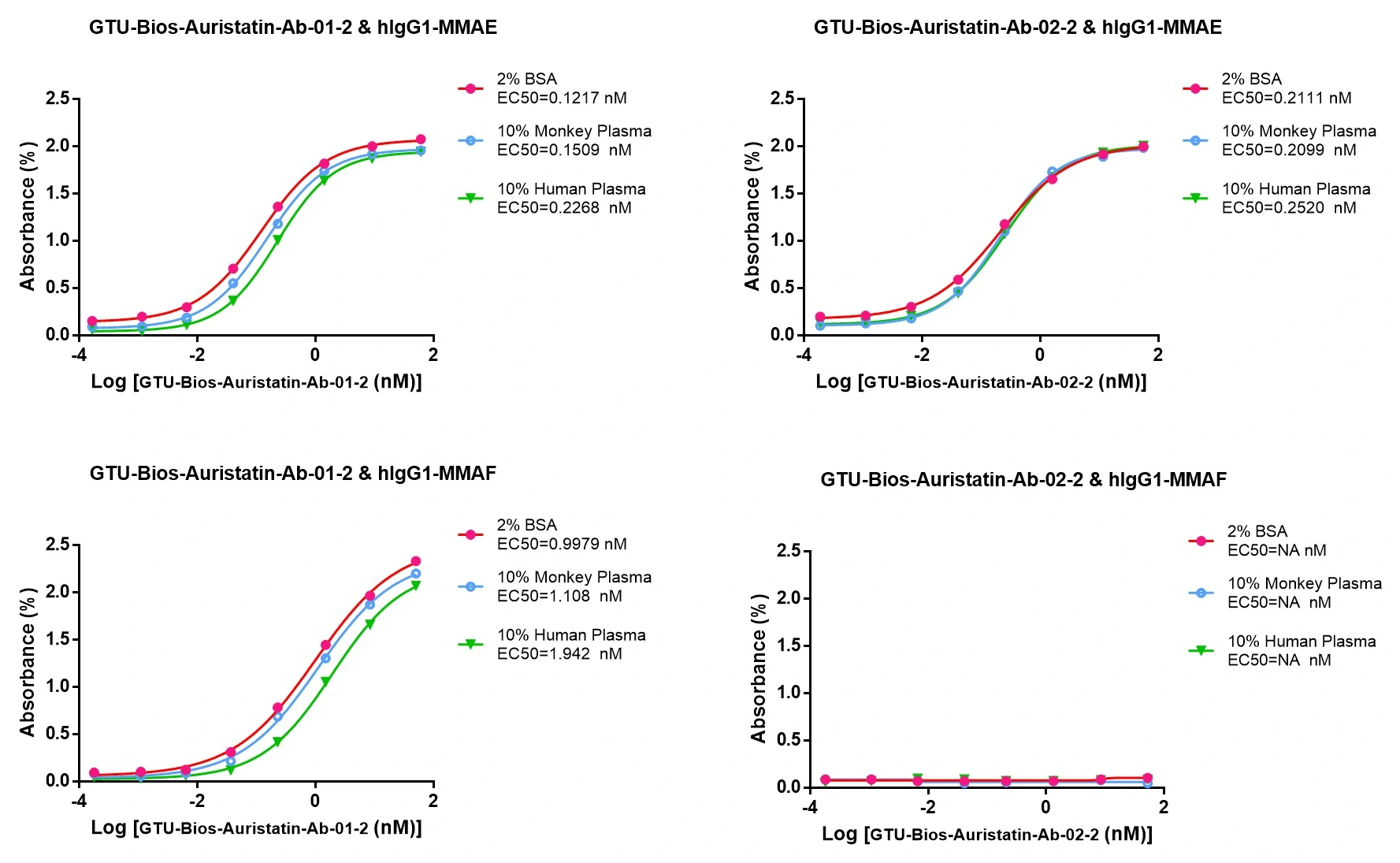
그림 4: GTU-Bios-Auristatin-Ab-01-2와 GTU-Bios-Auristatin-Ab-02-2는 인간 및 원숭이를 포함한 약동학(PK) 연구에 사용될 수 있습니다
GTU-Bios-Auristatin-Ab-01-2는 인간 및 원숭이 PK 연구에서 미미한 영향을 나타내며, 무시할 만합니다. GTU-Bios-Auristatin-Ab-02-2는 이러한 PK 연구에서 GTU-Bios-Auristatin-Ab-01-2보다도 영향이 적습니다. GTU-Bios-Auristatin-Ab-01-2와 GTU-Bios-Auristatin-Ab-02-2는 인간 및 원숭이 PK 실험에 적합합니다.
PK 연구에서 항-MMAE/MMAF 항체의 역할
-
검출 및 정량:
-
항-MMAE/MMAF 항체는 ADC 투여 후 방출되거나 순환 중에 남아 있는 MMAE/MMAF의 수준을 특이적으로 검출하고 정량하는 데 사용됩니다. 이는 ADC의 안정성과 약물 방출 속도를 평가하는 데 필수적입니다.
-
-
ADC 무결성 평가:
-
이 항체들을 사용하여 순환 중에 존재하는 자유 MMAE/MMAF를 측정함으로써, 연구자들은 ADC의 링커 안정성을 추론할 수 있습니다. 자유 약물의 농도가 높으면 링커가 덜 안정적임을 나타내어 세포독성 약물의 조기 방출로 이어질 수 있습니다.
-
-
안전성 및 효능 상관관계:
-
MMAE/MMAF의 약물동태학을 이해함으로써 약물 농도와 치료 효능 및 잠재적 독성을 상관시킬 수 있습니다. 항-MMAE/MMAF 항체는 다양한 생물학적 매트릭스에서 약물의 정확한 측정을 제공함으로써 이를 지원합니다.
-
-
면역원성 테스트:
-
ADC는 면역 반응을 유발하여 약물에 대한 항체(ADA)를 생성할 수 있으며, 이는 약물의 효능과 안전성에 영향을 미칠 수 있습니다. 항-MMAE/MMAF 항체는 약물 자체와 이에 대해 형성된 ADA를 구별하는 데 사용될 수 있습니다.
-
ADC 약물 개발에서의 응용
-
-
전임상 및 임상 개발: 전임상 및 임상 단계 모두에서 항-MMAE/MMAF 항체는 약물의 분포, 분해 및 제거를 모니터링하기 위한 분석에 사용됩니다. 이 정보는 투여 요법을 최적화하고 최소한의 독성으로 최대 치료 효능을 보장하는 데 중요합니다.
-
규제 준수: 이러한 항체를 사용한 PK 연구의 데이터는 약물의 체내 행동에 대한 자세한 정보를 제공함으로써 규제 요구 사항을 충족하는 데 도움이 되며, 이는 승인 절차에서 중요한 역할을 합니다.
-
제형 최적화: PK 연구에서 얻은 통찰력은 ADC의 제형 최적화에 도움이 됩니다. 예를 들어, MMAE/MMAF의 조기 방출이 관찰되는 경우 링커 화학이나 항체 자체의 변경을 고려하여 안정성을 향상시킬 수 있습니다.
-
따라서 PK 연구에서 항-MMAE/MMAF 항체의 사용은 MMAE/MMAF 기반 ADC의 성공적인 개발에 필수적이며, 초기 연구부터 임상 시험에 이르는 약물 개발의 많은 측면을 안내하는 중요한 데이터를 제공합니다.






 Facebook
Facebook LinkedIn
LinkedIn Twitter
Twitter
